Етан — це насичений вуглеводень, в молекулі якого атоми Карбону сполучені одинарним (простим) зв'язком.
Назва «етан» встановлена згідно з номенклатурою ІЮПАК. Префікс «ет-» посилається на присутність у карбоновому ланцюзі двох атомів вуглецю, а суфікс «-ан» — на присутність одинарного зв'язку між ними (тобто приналежність до алканів).
Етиле́н або ете́н (IUPAC) — С2Н4, найпростіший і найважливіший представник ряду ненасичених вуглеводнів з одним подвійним зв'язком.
Подвійний зв'язок між атомами Карбону в молекулі етилену виникає за рахунок утворення двох спільних електронних пар між атомами Карбону. Решта неспарених електронів кожного атома Карбону утворюють прості зв'язки з атомами Гідрогену. Отримали молекулу, склад якої С Н . Цю сполуку називають етин.
Етилен і ацетилен. Молекулярні та структурні формули, фізичні властивості.
| Ознака | Етилен (алкен) | Ацетилен (алкін) |
|---|---|---|
| Особливості будови | Має 1 подвійний зв'язок С=С | Має 1 потрійний зв'язок -С≡ С- |
| Молекулярна формула | С2Н4 | С2Н2 |
| Електронна формула | Н:С:::С:Н | |
| Структурна формула | Н Н С=С Н Н | Н – С ≡ С – Н |
2 бер. 2021 р.
Етилен реагує з воднем при нагріванні і за участю каталізатора. При цьому відбувається перетворення подвійного зв'язку між атомами Карбону на одинарний та приєднання по одному атому Гідрогену до кожного атома Карбону. Реакція гідрування також належить до реакцій приєднання. У результаті цієї реакції ми отримали етан.
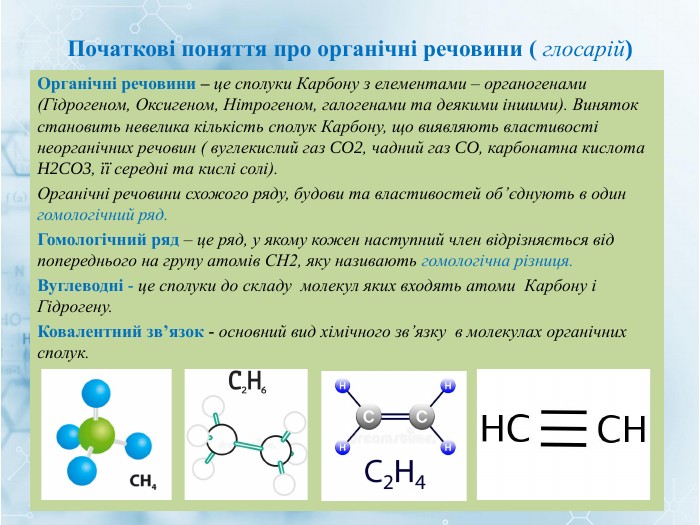

Отже, між атомами Карбону в молекулі етену утворюється подвійний зв’язок: один σ-, другий — π-зв’язок (мал. 32).